昨天,路透社、CNN、华尔街日报等媒体突发报道:
美国食药监局(FDA)批准了辉瑞疫苗的紧急使用授权,预计首次接种将在几日内展开。
CNN报道称,美国食品和药物管理局(FDA)已批准首批Covid-19疫苗在美国紧急使用。疫苗很快将在全国范围内运送,可能在之后几天内,就会开始接种疫苗。

《华尔街日报》报道称,鉴于迫切需要疫苗,FDA在几周内做出了决定,一般来说此类申请都需要几个月的时间来考虑。因而目前,FDA授予了临时许可,称之为紧急使用授权。

在《华尔街日报》的报道中,还阐述了目前疫苗的接种优先级。

第一优先级,1月可以接种疫苗的是,约2100万的卫生保健人员和300万承担长期护理工作的人员。
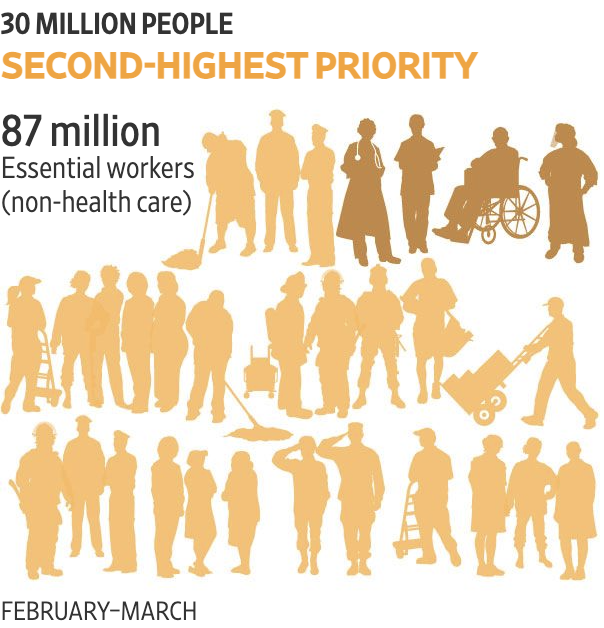
第二优先级,在2-3月可能会接种疫苗的是非护理医疗相关的工作人员。

第三优先级,为约1亿有高危健康风险的成年人和约5300万65岁以上的老人。

《华尔街日报》称,由于目前疫苗有限,辉瑞需要足够的时间来制作足够的剂量。因而对于大多数人来说,可能在春季或夏季之前都无法接种疫苗。
但无论如何,美国即将开始有史以来规模最大的疫苗接种运动。
辉瑞疫苗试验期间有6人死亡
尽管辉瑞疫苗的紧急使用被FDA批准了,但是近期其安全性却饱受质疑。
根据FDA的报告得知在辉瑞疫苗的试验后期有6人死亡,其中2人注射疫苗后死亡。

《联合早报》9日报道,美国食药监局的一会议文件显示,辉瑞在疫苗的后期试验中总共有六人死亡,其中两人注射疫苗后死亡。
据报道,两名注射疫苗后死亡的患者年龄高于55岁,其中一人原本已经患有动脉血管硬化,另一人则在注射第二剂疫苗的60天后心脏骤停。
而美国监管部门的报告显示:多名辉瑞疫苗的接种者出现了“面瘫”的情况。并且,有位接种疫苗的姑娘表示,感受到疫苗的副作用极大。
FDA则表示,这些死亡无关安全问题或疫苗有效性,因为所有事件都以相似的概率在普通人群中发生。

目前来看,瑞辉疫苗的临床试验参与者中,在接受注射后有63%的试验对象出现疲倦,有55%的人称他们患有头痛,32%的参与者表示发冷,24%的人抱怨关节疼痛,14%的人发烧。
欧洲两大制药巨头推迟新冠疫苗上市
以及同样是疫苗,欧洲两大制药巨头则表示要推迟上市!
据法新社巴黎消息,法国赛诺菲公司和英国葛兰素史克公司当地时间12月11日表示,这两家制药巨头合作研制的新冠病毒疫苗要到2021年底才能上市。
两家公司的声明称“一期和二期试验结果显示,18至49周岁受试者的免疫应答水平与新冠肺炎康复患者相似,但更高年龄段受试者的免疫应答水平较低,可能因为抗原浓度不足”。
因而,推迟上市是为了“提高中老年群体的免疫应答水平”,上市时间可能从2021年中推迟到第四季度。
赛诺菲巴斯德公司执行副总裁托马・特里翁夫说:
“我们非常关心公众健康。正因为如此,今天公布推迟上市的决定令我们自己倍感失望,但我们所有的决定都由科学和数据主导,未来也将如此。”
结 语
总的来说,美国FDA批准辉瑞新冠疫苗紧急使用授权对大多数人来说都是一件好事!医护人员和长期照护机构中的居民优先接种新冠疫苗,也能有效降低医疗体系内的病毒蔓延。美国疫情得到控制或许指日可待!
PS:虽然可能大多数人,暂时还不能在很短的时间内接种疫苗。但接种过的人越多也越安全不是吗!
但相关副作用也确实让一部分人望而生畏,小伙伴们如果有接种的需求,务必确认相关禁忌和注意事项哦!
最后,有关疫苗的最新消息小编都会及时跟进哒!




 炸裂!杭州美国留学中介最新排名震撼发布
炸裂!杭州美国留学中介最新排名震撼发布
